Zjawiska i procesy naturalne wokół nas są dość złożone. Do ich dokładnego opisu fizycznego należy zastosować niewygodny aparat matematyczny i wziąć pod uwagę dużą liczbę istotnych czynników. Aby uniknąć tego problemu, w fizyce stosuje się uproszczone modele, które znacznie ułatwiają matematyczną analizę procesu, ale praktycznie nie wpływają na dokładność jego opisu. Jednym z nich jest model gazu idealnego. Rozważmy to bardziej szczegółowo w artykule.
Koncepcja gazu doskonałego
Gaz doskonały to stan skupienia substancji, który składa się z punktów materialnych, które nie oddziałują ze sobą. Wyjaśnijmy tę definicję bardziej szczegółowo.
Po pierwsze, mówimy o punktach materialnych jako obiektach, które składają się na gaz doskonały. Oznacza to, że jego cząsteczki i atomy nie mają rozmiaru, ale mają określoną masę. To odważnemożna dokonać przybliżenia, biorąc pod uwagę fakt, że we wszystkich rzeczywistych gazach przy niskich ciśnieniach i wysokich temperaturach odległość między cząsteczkami jest znacznie większa niż ich wymiary liniowe.
Po drugie, cząsteczki gazu doskonałego nie powinny ze sobą oddziaływać. W rzeczywistości takie interakcje istnieją zawsze. Tak więc nawet atomy gazów szlachetnych doświadczają przyciągania dipol-dipol. Innymi słowy, interakcje van der Waalsa są obecne. Jednak w porównaniu z energią kinetyczną rotacji i ruchem translacyjnym cząsteczek, oddziaływania te są tak małe, że nie wpływają na właściwości gazów. Dlatego nie można ich brać pod uwagę przy rozwiązywaniu praktycznych problemów.
Ważne jest, aby pamiętać, że nie wszystkie gazy o niskiej gęstości i wysokiej temperaturze można uznać za idealne. Oprócz oddziaływań van der Waalsa istnieją inne, silniejsze typy wiązań, na przykład wiązania wodorowe między cząsteczkami H2O, które prowadzą do rażącego naruszenia warunków idealności gazu. Z tego powodu para wodna nie jest gazem idealnym, ale powietrze jest.
Fizyczny model gazu doskonałego
Ten model można przedstawić w następujący sposób: załóżmy, że system gazowy zawiera cząstki N. Mogą to być atomy i cząsteczki różnych chemikaliów i pierwiastków. Liczba cząstek N jest duża, więc do jej opisu zwykle używa się jednostki „mol” (1 mol odpowiada liczbie Avogadro). Wszystkie poruszają się w pewnej objętości V. Ruchy cząsteksą chaotyczne i niezależne od siebie. Każdy z nich ma określoną prędkość v i porusza się po prostej ścieżce.
Teoretycznie prawdopodobieństwo kolizji między cząstkami jest prawie zerowe, ponieważ ich rozmiar jest mały w porównaniu do odległości między cząstkami. Jeśli jednak dojdzie do takiej kolizji, to jest ona absolutnie elastyczna. W tym drugim przypadku całkowity pęd cząstek i ich energia kinetyczna są zachowane.
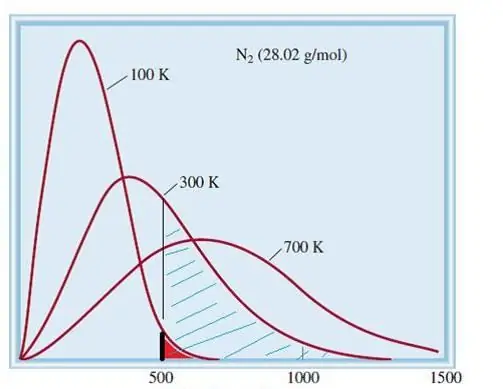
Rozważany model gazów doskonałych to klasyczny układ z ogromną liczbą pierwiastków. Dlatego prędkość i energia zawartych w nim cząstek są zgodne z rozkładem statystycznym Maxwella-Boltzmanna. Niektóre cząstki mają niskie prędkości, podczas gdy inne mają wysokie prędkości. W tym przypadku istnieje pewne wąskie ograniczenie prędkości, w którym leżą najbardziej prawdopodobne wartości tej wielkości. Rozkład prędkości cząsteczek azotu pokazano schematycznie poniżej.
Kinetyczna teoria gazów
Opisany powyżej model gazów doskonałych jednoznacznie określa właściwości gazów. Model ten został po raz pierwszy zaproponowany przez Daniela Bernoulliego w 1738 roku.

Później został opracowany do obecnego stanu przez Augusta Kroeniga, Rudolfa Clausiusa, Michaiła Łomonosowa, Jamesa Maxwella, Ludwiga Boltzmanna, Mariana Smoluchowskiego i innych naukowców.
Teoria kinetyczna substancji płynnych, na podstawie której budowany jest model gazu doskonałego, wyjaśnia dwie ważne makroskopowe właściwości układu w oparciu o jego zachowanie mikroskopowe:
- Ciśnienie gazów jest wynikiem zderzenia cząstek ze ścianami naczynia.
- Temperatura w układzie jest wynikiem ciągłego ruchu cząsteczek i atomów.
Rozwińmy oba wnioski teorii kinetycznej.
Ciśnienie gazu
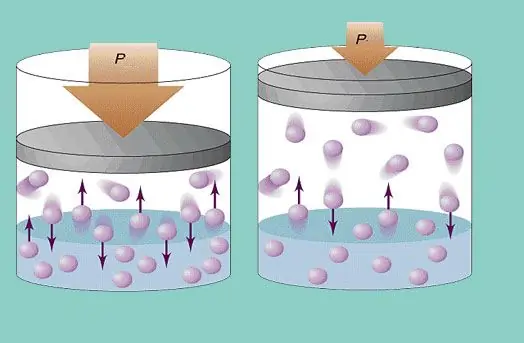
Model gazu doskonałego zakłada stały chaotyczny ruch cząstek w układzie i ich ciągłe zderzenia ze ścianami naczynia. Każda taka kolizja jest uważana za całkowicie elastyczną. Masa cząstek jest mała (≈10-27-10-25 kg). Dlatego nie może wytworzyć dużego nacisku podczas kolizji. Niemniej jednak liczba cząstek, a co za tym idzie liczba zderzeń, jest ogromna (≈1023). Ponadto średnia kwadratowa prędkość pierwiastków wynosi kilkaset metrów na sekundę w temperaturze pokojowej. Wszystko to prowadzi do powstania znacznego nacisku na ściany naczynia. Można go obliczyć za pomocą następującego wzoru:
P=Nmvcp2 / (3V), gdzie vcp to średnia kwadratowa prędkość, m to masa cząstki.
Temperatura absolutna
Zgodnie z modelem gazu doskonałego, temperatura jest jednoznacznie określona przez średnią energię kinetyczną cząsteczki lub atomu w badanym układzie. Możesz napisać następujące wyrażenie, które wiąże energię kinetyczną i temperaturę bezwzględną dla gazu doskonałego:
mvcp2 /2=3 / 2kB T.
Tutaj kB jest stałą Boltzmanna. Z tej równości otrzymujemy:
T=m vcp2 / (3kB).
Uniwersalne równanie stanu
Jeśli połączymy powyższe wyrażenia dla ciśnienia bezwzględnego P i temperatury bezwzględnej T, możemy zapisać następującą równość:
PV=nRT.
Tutaj n jest ilością substancji w molach, R jest stałą gazową wprowadzoną przez D. I. Mendelejewa. Wyrażenie to jest najważniejszym równaniem w teorii gazów doskonałych, ponieważ łączy w sobie trzy parametry termodynamiczne (V, P, T) i nie zależy od właściwości chemicznych układu gazowego.

Uniwersalne równanie zostało najpierw eksperymentalnie wyprowadzone przez francuskiego fizyka Emila Clapeyrona w XIX wieku, a następnie doprowadzone do jego nowoczesnej postaci przez rosyjskiego chemika Mendelejewa, dlatego obecnie nosi ono nazwiska tych naukowców.






