Termodynamika to ważna gałąź fizyki. Można śmiało powiedzieć, że jego osiągnięcia doprowadziły do nastania ery technologicznej i w dużej mierze zdeterminowały bieg historii ludzkości na przestrzeni ostatnich 300 lat. W artykule omówiono pierwszą, drugą i trzecią zasadę termodynamiki oraz ich zastosowanie w praktyce.
Co to jest termodynamika?
Przed sformułowaniem praw termodynamiki zastanówmy się, co robi ta sekcja fizyki.
Słowo „termodynamika” ma greckie pochodzenie i oznacza „ruch pod wpływem ciepła”. Oznacza to, że ta gałąź fizyki zajmuje się badaniem wszelkich procesów, w wyniku których energia cieplna jest przekształcana w ruch mechaniczny i odwrotnie.
Podstawowe prawa termodynamiki zostały sformułowane w połowie XIX wieku. Nauka o „ruchu i cieple” rozważa zachowanie całego układu jako całości, badając zmianę jego parametrów makroskopowych - temperatury, ciśnienia i objętości, nie zwracając uwagi na jego strukturę mikroskopową. Co więcej, pierwszy z nich odgrywa fundamentalną rolę w formułowaniu prawatermodynamika w fizyce. Warto zauważyć, że pochodzą one wyłącznie z obserwacji eksperymentalnych.
Koncepcja systemu termodynamicznego

Oznacza to dowolną grupę atomów, cząsteczek lub innych pierwiastków, które są traktowane jako całość. Wszystkie trzy prawa są sformułowane dla tzw. układu termodynamicznego. Przykładami są: atmosfera ziemska, dowolny żywy organizm, mieszanina gazów w silniku spalinowym itp.
Wszystkie systemy w termodynamice należą do jednego z trzech typów:
- Otwórz. Wymieniają ciepło i materię z otoczeniem. Na przykład, jeśli jedzenie jest gotowane w garnku na otwartym ogniu, jest to żywy przykład systemu otwartego, ponieważ garnek otrzymuje energię ze środowiska zewnętrznego (ogień), podczas gdy sam emituje energię w postaci ciepła, woda również z niej odparowuje (metabolizm).
- Zamknięte. W takich układach nie ma wymiany materii z otoczeniem, chociaż następuje wymiana energii. Wracając do poprzedniego przypadku: jeśli przykryjesz czajnik pokrywką, możesz uzyskać system zamknięty.
- Odizolowane. Jest to rodzaj układów termodynamicznych, które nie wymieniają materii ani energii z otaczającą przestrzenią. Przykładem może być termos z gorącą herbatą.
Temperatura termodynamiczna

Ta koncepcja oznacza energię kinetyczną cząstek tworzących otaczające ciała, która odzwierciedla prędkośćprzypadkowy ruch cząstek. Im jest większy, tym wyższa temperatura. W związku z tym, zmniejszając energię kinetyczną układu, chłodzimy go.
To pojęcie oznacza energię kinetyczną cząstek tworzących otaczające ciała, która odzwierciedla prędkość chaotycznego ruchu cząstek. Im jest większy, tym wyższa temperatura. W związku z tym, zmniejszając energię kinetyczną układu, chłodzimy go.
Temperatura termodynamiczna jest wyrażana w SI (Międzynarodowy Układ Jednostek) w Kelvinach (na cześć brytyjskiego naukowca Williama Kelvina, który jako pierwszy zaproponował tę skalę). Zrozumienie pierwszej, drugiej i trzeciej zasady termodynamiki jest niemożliwe bez definicji temperatury.
Podział jednego stopnia w skali Kelvina również odpowiada jednemu stopniowi Celsjusza. Przeliczenie pomiędzy tymi jednostkami odbywa się według wzoru: TK =TC + 273, 15, gdzie TK i TC - temperatury odpowiednio w kelwinach i stopniach Celsjusza.
Specyfika skali Kelvina polega na tym, że nie ma ona wartości ujemnych. Zero w nim (TC=-273, 15 oC) odpowiada stanowi, w którym ruch termiczny cząstek układu jest całkowicie nieobecny, wyglądają na „zamrożone”.
Zachowanie energii i I zasada termodynamiki

W 1824 roku Nicolas Léonard Sadi Carnot, francuski inżynier i fizyk, wysunął śmiałą sugestię, która nie tylko doprowadziła do rozwoju fizyki, ale także stała się ważnym krokiem w ulepszaniu technologii. Jegomożna sformułować w następujący sposób: "Energia nie może być tworzona ani niszczona, może być tylko przenoszona z jednego stanu do drugiego."
W rzeczywistości zdanie Sadi Carnota postuluje prawo zachowania energii, które stanowi podstawę I zasady termodynamiki: „Za każdym razem, gdy system otrzymuje energię z zewnątrz, przekształca ją w inne formy, główne które są termiczne i mechaniczne."
Matematyczny wzór pierwszego prawa jest zapisany w następujący sposób:
Q=ΔU + A, tutaj Q to ilość ciepła przekazywanego przez otoczenie do systemu, ΔU to zmiana energii wewnętrznej tego systemu, A to doskonała praca mechaniczna.
Procesy adiabatyczne
Dobrym przykładem jest ruch mas powietrza po zboczach gór. Takie masy są ogromne (kilometrów lub więcej), a powietrze jest doskonałym izolatorem ciepła. Zanotowane właściwości pozwalają uznać za adiabatyczne dowolne procesy z masami powietrza, które zachodzą w krótkim czasie. Kiedy powietrze unosi się w górę zbocza góry, jego ciśnienie spada, rozszerza się, to znaczy wykonuje pracę mechaniczną, w wyniku czego ochładza się. Przeciwnie, ruchowi masy powietrza w dół towarzyszy wzrost w nim ciśnienia, ściska się i przez to staje się bardzo gorący.
Zastosowanie prawa termodynamiki, które zostało omówione w poprzednim podtytule, najłatwiej zademonstrować na przykładzie procesu adiabatycznego.
Zgodnie z definicją w wyniku tego nie dochodzi do wymiany energii zśrodowisko, czyli w powyższym równaniu Q=0. Prowadzi to do następującego wyrażenia: ΔU=-A. Znak minus oznacza tutaj, że system wykonuje pracę mechaniczną, zmniejszając swoją własną energię wewnętrzną. Należy przypomnieć, że energia wewnętrzna jest bezpośrednio zależna od temperatury układu.
Kierunek procesów termicznych
To wydanie dotyczy drugiej zasady termodynamiki. Zapewne wszyscy zauważyli, że jeśli zetkniesz dwa przedmioty o różnych temperaturach, to zimny zawsze będzie się nagrzewał, a gorący ostygnie. Zauważ, że proces odwrotny może zachodzić w ramach pierwszej zasady termodynamiki, ale nigdy nie jest realizowany w praktyce.
Powodem nieodwracalności tego procesu (i wszystkich znanych procesów we Wszechświecie) jest przejście układu do bardziej prawdopodobnego stanu. W rozważanym przykładzie ze stykiem dwóch ciał o różnych temperaturach najbardziej prawdopodobnym stanem będzie taki, w którym wszystkie cząstki układu będą miały tę samą energię kinetyczną.
Drugie prawo termodynamiki można sformułować w następujący sposób: „Ciepło nigdy nie może zostać przeniesione z zimnego ciała do gorącego”. Jeśli wprowadzimy pojęcie entropii jako miary nieporządku, to można je przedstawić w następujący sposób: „Każdy proces termodynamiczny przebiega ze wzrostem entropii”.
Silnik cieplny

Pod tym pojęciem rozumie się system, który dzięki dostarczeniu do niego energii zewnętrznej może wykonywać pracę mechaniczną. Pierwszymaszyny cieplne były maszynami parowymi i zostały wynalezione pod koniec XVII wieku.
Druga zasada termodynamiki odgrywa decydującą rolę w określaniu ich skuteczności. Sadi Carnot ustalił również, że maksymalna wydajność tego urządzenia to: Wydajność=(T2 - T1)/T2, tutaj T2 i T1 to temperatury grzejnika i lodówki. Praca mechaniczna może być wykonywana tylko wtedy, gdy występuje przepływ ciepła z gorącego ciała do zimnego, a przepływ ten nie może być w 100% przekształcony w energię użyteczną.
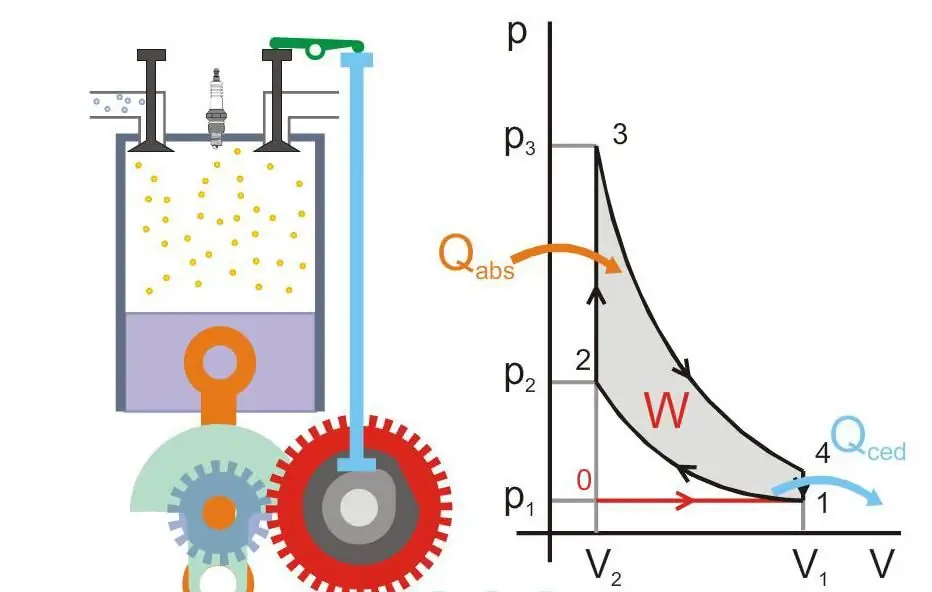
Poniższy rysunek przedstawia zasadę działania silnika cieplnego (Qabs - ciepło przekazywane do maszyny, Qced - straty ciepła, W - praca użyteczna, P i V - ciśnienie i objętość gazu w tłoku).
Zero absolutne i postulat Nernsta
Na koniec przejdźmy do rozważenia trzeciej zasady termodynamiki. Nazywany jest także postulatem Nernsta (od nazwiska niemieckiego fizyka, który jako pierwszy go sformułował na początku XX wieku). Prawo mówi: „Zera absolutnego nie można osiągnąć za pomocą skończonej liczby procesów”. Oznacza to, że w żaden sposób nie można całkowicie „zamrozić” cząsteczek i atomów substancji. Powodem tego jest stała wymiana ciepła z otoczeniem.

Jednym z użytecznych wniosków wyciągniętych z trzeciej zasady termodynamiki jest to, że entropia maleje w miarę zbliżania się do zera absolutnego. Oznacza to, że system sam się organizuje. Ten fakt możeużywać na przykład do przenoszenia paramagnesów do stanu ferromagnetycznego po schłodzeniu.
Ciekawe, że najniższa jak dotąd osiągnięta temperatura to 5·10−10 K (2003, laboratorium MIT, USA).






